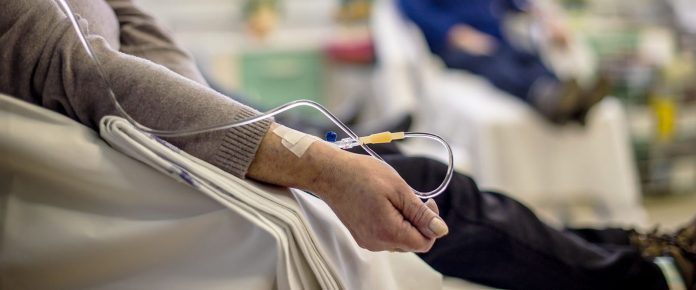
Cancerul este o luptă intensă între tratamente agresive și supraviețuirea pacientului. Printre cele mai utilizate arme, chimioterapia joacă un rol esențial, vizând celulele canceroase care se divid rapid. Totuși, persistă un paradox: deși distrug tumorile, aceste medicamente pot afecta și celulele sănătoase, în special pe cele care se reînnoiesc frecvent, cum sunt celulele sanguine. Un nou studiu publicat în Nature Genetics aduce o perspectivă fără precedent asupra acestei „sabii cu două tăișuri”, dezvăluind modul în care anumite tratamente accelerează artificial îmbătrânirea celulelor sănătoase – în funcție de tipul medicamentului administrat.
Chimioterapia acționează prin provocarea de rupturi și mutații în ADN-ul celular, determinând moartea celulelor tumorale. Însă celulele normale – în special celulele stem din sânge – care se divid rapid, pot suferi la rândul lor daune genetice, ducând la acumularea de mutații în timp. Pentru a evalua cu precizie aceste efecte, cercetătorii au analizat probe de sânge de la 23 de pacienți tratați cu diverse protocoale chimioterapice, comparându-le cu cele ale unui grup de control format din nouă persoane sănătoase. Abordarea lor inovatoare a constat în izolarea și secvențierea ADN-ului din celulele stem hematopoietice, pentru a identifica „semnături mutaționale” – modele distincte de mutații asociate cu daunele provocate de anumite medicamente.
Studiul a identificat patru semnături mutaționale noi, necunoscute anterior în baza de date globală COSMIC. Aceste mutații au fost detectate exclusiv la pacienții tratați și variau în funcție de tipul de chimioterapie. De exemplu, unii agenți alchilanți și compușii pe bază de platină s-au dovedit responsabili pentru un număr mare de mutații, în timp ce alte medicamente, precum ciclofosfamida, au generat mult mai puține modificări genetice – ceea ce ar putea explica de ce riscul de cancer secundar este mai scăzut în cazul acestora.
Acumularea de mutații în ADN este un proces natural asociat cu îmbătrânirea. Însă la pacienții care au urmat tratamente chimioterapice, această îmbătrânire genetică este accelerată. Un exemplu remarcabil din studiu: un copil de trei ani supus chimioterapiei a prezentat de zece ori mai multe mutații în celulele sale sanguine decât copiii sănătoși de aceeași vârstă. Mai mult, la nivel genetic, celulele sale păreau mai „bătrâne” decât cele ale unei persoane de 80 de ani care nu primise tratament. Această îmbătrânire prematură nu implică automat dezvoltarea unui nou cancer, dar crește riscul apariției tumorilor secundare – un aspect crucial în monitorizarea pacienților pe termen lung, mai ales a celor care supraviețuiesc ani întregi după tratamentul inițial.
Aceste descoperiri ar putea conduce la o selecție mai atentă a protocoalelor chimioterapice. Prin identificarea tratamentelor care produc mai puține mutații, medicii ar putea alege terapii care păstrează eficiența împotriva cancerului, dar sunt mai blânde cu celulele sănătoase. Deja, în anumite forme de limfom Hodgkin, s-au testat combinații alternative de chimioterapie care reduc semnificativ numărul de mutații secundare, fără a compromite șansele de vindecare. Acest lucru este cu atât mai important în cancerele cu rată mare de supraviețuire, unde reducerea efectelor pe termen lung devine prioritară. În cazurile mai agresive, unde șansele de vindecare sunt mai mici, obiectivul principal rămâne eliminarea cancerului, chiar cu prețul unei toxicități mai ridicate. După cum subliniază un expert de la Centrul de Cancer Memorial Sloan Kettering: „Mai întâi trebuie să vindecăm boala, apoi putem reduce toxicitatea.”
Desigur, studiul are și limitări. Dimensiunea relativ mică a eșantionului și faptul că analizele s-au efectuat în laborator, pe celule izolate, nu reproduc cu totul complexitatea mediului uman. Cercetătorii intenționează să-și extindă investigațiile la cohorte mai mari, folosind inclusiv sânge circulant.
Chiar și așa, această cercetare marchează un progres major în înțelegerea efectelor secundare genetice ale chimioterapiei și ar putea deschide drumul către o medicină mai personalizată – una care combină eficiența terapeutică cu protejarea celulelor sănătoase ale pacientului.
Poll: Care este cel mai important aspect de luat în considerare în alegerea protocoalelor chimioterapice?


Revista “Ştiinţă şi Tehnică“, cea mai cunoscută şi longevivă publicaţie de popularizare a ştiintelor din România




















Leave a Reply