A fost un drum lung, cel care a dus la înțelegerea existenței unei ordini în elementele chimice. Un drum care, sunt convins de asta, ilustrează foarte bine însăși evoluția științei, de la mistere filosofice, la o mai bună înțelegere a lumii. Ne apropiem cu pași iuți de momentul astral al descoperirii lui Mendeleev.
La jumătatea secolului al XIX-lea chimia era în plină efervescență. Deja bazele ei deveniseră suficient de solide, ceea ce lăsa loc unei evoluții rapide. Se dezvolta rapid și chimia organică. Totuși erau multe întrebări care nu își găsiseră răspunsul. Ar fi fost greu să fie găsite, câtă vreme oamenii de știință nu aveau, încă, un model fizic acceptabil al atomilor. Acesta avea să se contureze către sfârșitul secolului XIX și începutul secolului XX.
Totuși savanții vremii încercau să găsească o anumită ordine care ar guverna elementele chimice. Inspirați probabil de biologie, care dispunea de o clasificare organismelor, se încerca gruparea elementelor chimice în funcție de diferite criterii.
O primă clasificare a elementelor chimice a fost făcută de însuși Lavoisier. El a încercat să le grupeze în funcție de natura combinațiilor chimice pe care acestea le formau cu oxigenul. În 1816, Ampere, propune o clasificare similară cu cea propusă de Carl Linnaeus pentru plante. Ampere considera fiecare element chimic ca fiind o specie. Speciile erau grupate în genuri, iar genurile în familii. De exemplu, clasa ”Leucolyte” conținea genul ”Calcide”, din care făceau parte patru specii: bariul, stronțiul, calciul și magneziul.
Părea natural ca, în încercarea de clasificare a elementelor chimice, să intre în joc și masa atomică a lor. După știința mea, o primă încercare a fost făcută de către chimistul german Johann Wolfgang Döbereiner.
Triadele lui Döbereiner
În 1816 Döbereiner constata faptul că masa atomică a stronțiului era foarte apropiată de media aritmetică maselor atomice ale calciului și bariului, iar aceste trei elemente chimice au anumite propietăți asemănătoare. Tot el semnala, în cursurile sale de la Universitatea Jena, faptul că bromul, proaspăt descoperit, în 1825, ar trebui, la rândul său, să aibă o masă atomică egală cu media aritmetică dintre masa atomică a clorului și iodului. Predicția i-a fost confirmată de Berzelius, în 1826.
Döbereiner era convins că există mai multe grupări de trei elemente chimice, pe care el le-a numit triade, în care putem regăsi aceleași proprietăți. În afară de cele două de mai sus, el nu a mai identiticat decât una: sulf, seleniu și teluriu.
A încercat să găsească și alte triade, dar căutările lui s-au soldat cu un eșec. Din acest motiv, chimiștii vremii au considerat că avem de-a face cu o simplă coincidență lipsită de însemnătate. Așa cum scria Asimov în cartea pe care am citat-o în primul episod al serialului nostru (A short History of Chemistry), ”În prima jumătate a secolului al XIX-lea, [importanța] masei atomice era subestimată. Era convenabilă pentru a face anumite calcule, dar nu părea să fie vreun motiv pentru ca ea să fie folosită [la altceva decât la o] listă elementelor chimice.”
Lucrurile aveau să se schimbe dramatic în deceniile următoare. O idee plutea în aer.
Cilindrul lui Beguyer de Chancourtois
Francezul Beguyer de Chancourtois era un geolog renumit. În 1862, publică lucrarea intitulată ”Mémoire sur un classement naturel des corps simples ou radicaux appelé vis tellurique” (Memoriu asupra unui clasament al corpurilor simple sau radicale, intitulat șurubul teluric). Da, aveți dreptate. Titlul nu pare a fi deloc promițător. Totuși el a fost foarte aproape de a realiza primul tabel periodic al elementelor chimice.

De Chancourtois a plasat elementele chimice cunoscute pe o spirală, în funcție de ceea ce el numea ”numere caracteristice” sau ”caractere numerice”. Din conetxt rezultă că este vorba despre masele atomice corespunzătoare. Grafic, el a construit un cilindru a cărui bază circulară era împărțită în 16 părți egale. Pe acest cilindru el a desenat o spirală, care făcea un unghi de 45° față de generatoare. Fiecare tură completă a acestei spirale a fost împărțită, la rândul ei, tot în 16 părți egale. Pe această spirală au fost marcate punctele corespunzătoare maselor atomice ale elementelor chimice cunoscute în vremea sa. Vă cer un mic efort. Sper că puteți să vă reprezentați în minte cilindrul și spirala lui de Chancourtois. La fiecare 360°, spirala intersectează aceeași generatoare a cilindrului. Drept urmare, elementele chimice ale căror mase atomice difereau cu 16 unități se aflau unul deasupra celuilalt, pe aceeași linie verticală. De exemplu, sodiul, al cărui masă atomică este egală circa 23 de unități, îl vom găsi plasat pe aceeași linie verticală cu litiul, a cărui masă atomică este de circa 7 unități. De Chancourtois a putut constata că elementele chimice aflate pe aceași generatoare împărtășesc proprietăți chimice similare. Făcuse un pas important către găsirea unei căi de ordonare a elementelor chimice.
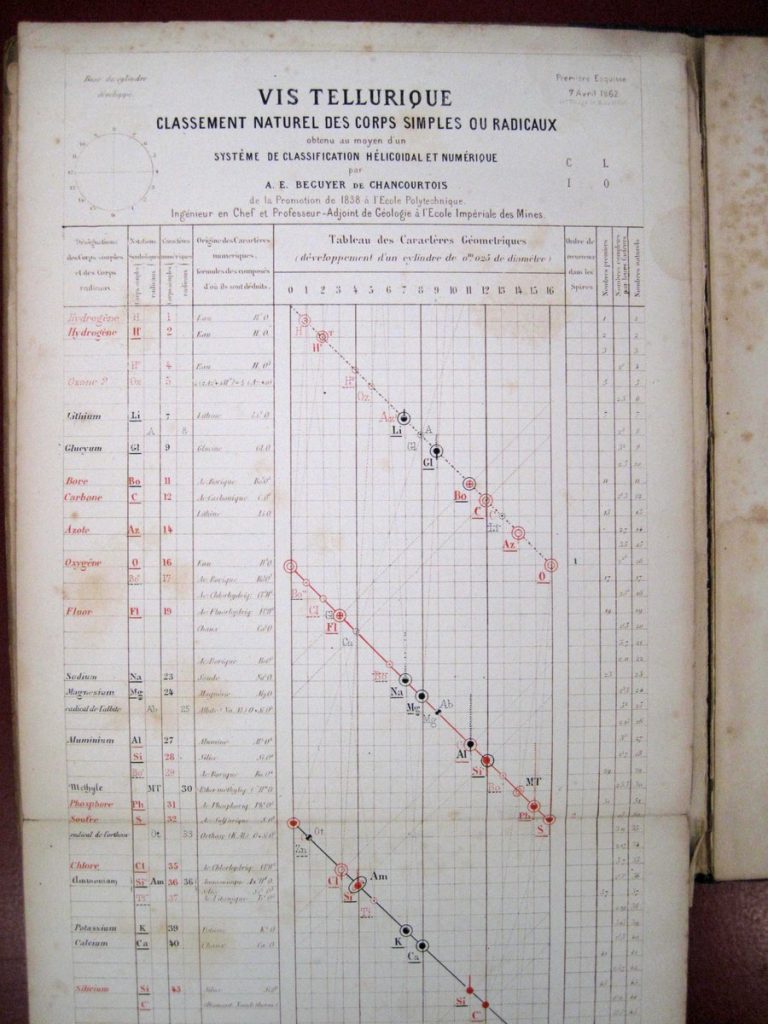
Din nefericire, din mai multe motive, pasul acesta a trecut neobservat. În primul rând de Chancourtois era geolog, iar chimiștii nu prea erau preocupați de lucrările scrise de aceștia. În al doilea rând, limbajul folosit de el este adesea neclar. De exemplu, nu am găsit în textul său referiri directe la masa atomică, ci numai referiri la ”numere caracteristice” și ”caractere numerice”. În al treilea rând, în ”Mémoire sur un classement naturel des corps simples ou radicaux appelé vis tellurique” nu există nici măcar o figură care să ilustreze spirala elementelor chimice despre care vorbește. Sunt convins că ea ar fi clarificat foarte mult expunerea lui de Chancourtois.
Ideea periodicității elementelor chimice plutea în continuare în aerul tumultos al științei.
John Alexander Reina Newlands
Englezul John Newlands, la rândul său, a fost la o singură aruncătură de băț de marea descoperire.
Între 1863 și 1866 el publică o serie de articole în care prezenta tabele în care elementele chimice erau grupate în tabele ale căror coloane conțineau câte șapte elemente chimice, ordonate după masa atomică. Astfel a putut arăta că elemente chimice care se află pe aceași linie au proprietăți similare. Astfel, pe aceeași linie, în două coloane alăturate, găsim sodiul și potasiul, la fel se întâmplă cu seleniul și sulful, cu calciul și magneziul și așa mai departe.

Newlands afirmă că există o lege a ordonării chimice, pe care el a numit-o „legea octavelor”. El o explică astfel în ”On the Law of Octaves”, articol publicat în 1865. ”Se vede de asemenea că numărul corespunzător elementelor chimice [cu proprietăți similare] diferă cu 7 sau cu un multiplu de 7. Cu alte cuvinte, membrii aceluiași grup sunt în aceeași relație ca extremitățile uneia sau mai multor octave din muzică. Al optulea element pornind de la un element dat este un fel de repetiție al primului. Propun ca această relație particulară să poarte numele de lege a octavelor.” Din nefericire, în timp ce pe unele linii găsim elemente chimice cu proprietăți similare, în altele nu se mai întâmplă același lucru. El nu a avut curajul să lase spații libere pentru elementele care ar fi trebui să fie prezente acolo, dar care încă nu fuseseră descoperite încă, așa cum avea să facă Mendeleev în 1869.
Oricum, deși se apropiase foarte mult de descoperirea periodicității proprietăților elementelor chimice, lucrările lui nu au fost bine primite nici măcar de către colegii din Marea Britanie. La o conferință a Chemical Society, în care s-au dezbătut ideile sale, Newlands a fost întrebat de ce nu a încercat o grupare a elementelor chimice în ordine alfabetică, de vreme ce orice aranjament ar putea scoate la iveală coincidențe întâmplătoare.
Dar, în ciuda respingerii ideilor lui Newlands, revoluția plutea în aer.
Intermezzo
Da, ideea plutea în aer, ne dăm seama mai ales acum la un veac și jumătate de la revoluția declanșată de către Mendeleev. V-am dat doar câteva exemple de oameni care ar fi putut să o declanșeze înaintea lui, dar aș fi putut să vă dau mai multe. Acesta era spiritul timpului acela. Se acumulaseră datele necesare și era nevoie doar de un om care să le conecteze cum trebuie. Din întâmplare, sau nu, el a fost Mendeleev.
Dar cât de lung a fost drumul până s-a ajuns la acest moment crucial! Vă rog să recitiți episoadele anterioare. De la descoperiri întâmplătoare, care păreau a ține de magie, de la explicații filosofice, lipsite de sens și totuși minunate, de la căutarea pietrei filosofale, care ne-ar aduce nemurirea, de la dorința de a transmuta elemente în aur și până la acest moment, în care în aer plutește o mare revoluție, totul este o minunată istorie a gândirii umane. Cred că se cuvine să medităm îndelung asupra ei. Și aici nu mă gândesc numai la istoria chimiei, ci la cea a științei în general. Este o istorie în care găsim o adevărată aventură a umanității, prin care încet, dar sigur, vom ajunge să cuprindem cu mintea noastră întreg Universul. O aventură care a implicat adesea răsturnări ale unor concepte care păreau a ține de bunul simț comun, o luptă continuă în care, alături de rațiune, am înțeles că trebuie folosite dovezile drept armă, pentru tranșarea disputelor.
Suntem acum, în a doua jumătate a secolului al XIX-lea, în momentul în care se acumulaseră suficiente dovezi pentru a se trece la următorul pas: revoluția. Este adevărat, așa cum am mai spus, deși oamenii de știință acceptau modelul atomic, nu se știa mai nimic despre structura acestuia. Asta era un mare dezavantaj. Datele despre proprietațile chimice ale elementelor erau pur empirice, deși deveniseră din ce în ce mai precise. Tot precise deveniseră și determinările de mase atomice. Dar, pentru o bună înțelegere a reacțiilor chimice, era nevoie și de un model atomic fiabil. Vă spun toate astea pentru a sublinia importanța revoluției ce stătea să izbucnească. Consecințele ei depășesc cu mult domeniul chimiei. O dată ordinea descoperită, urma întrebarea firească pentru oamenii de știință: care este mecanismul care generează această ordine? Răspunsul a fost găsit de către fizicienii care cercetau alte fenomene, inexplicabile la momentul descoperirii lor. Îmi dau seama, vă duc într-o altă poveste. O mică parte din ea v-am spus-o pe parcursul a aproape trei decenii, de când am avut privilegiul pe a o așterne în scris.
Încheiere provizorie
M-am lăsat purtat de cuvinte. De aceea le părăsesc pe ale mele. Uitați ce scrie Leonard Mlodinow, în Odiseea umană, traducere publicată de Editura Herald în 2018. ”Privind în urmă, este ușor să explicăm realizarea lui Mendeleev prin aceea că a pus întrebarea potrivită la momentul potrivit, prin etica muncii, pasiunea, încăpățânarea și extrema încredere în sine. Dar, așa cum se întâmplă în descoperire și inovație – și de multe ori în viața noastră – la fel de important precum calitățile intelectuale a fost rolul întâmplării, sau cel puțin o împrejurare fără legătură care a pregătit terenul ca aceste calități să poată triumfa. În cazul de față a fost decizia întâmplătoare a lui Mendeleev de a scrie un tratat de chimie.”
Despre Mendeelev, și despre revoluția declanșată de el, vă voi povesti în numărul viitor.
Episodul 1 al serialului îl găsiți aici.
Episodul 2 al serialului îl găsiți aici.
Episodul 3 al serialului îl găsiți aici.
Episodul 4 al serialului îl găsiți aici.
Episodul 6 al serialului îl găsiți aici


Cristian Român (n. 1957) este inginer de aeronave și, începând din 1992, jurnalist de știință. Scrie pentru revista Știință și Tehnică și a realizat numeroase emisiuni de popularizare a științei atât pentru televiziune, cât și pentru radio. Este autorul cărții Ultima aventura: Universul. Valoarea textelor sale i-a fost recunoscută prin acordarea, în 2003 și 2006, a Premiului Comisiei Naționale a României pentru UNESCO pentru jurnalismul de știință, secțiunea presă scrisă. De asemenea el a primit Petre Sergescu al Academiei Române pentru cartea ”100 de inovatori români”, al cărei coautor a fost.